“이쪽에서 전자가 나가고, 저쪽에서 받아들인다”… 그걸 뭐라고 부를까?
전기화학을 조금이라도 공부하다 보면
늘 등장하는 두 단어가 있습니다: 산화와 환원.
산화? 환원?
산소와 관련 있는 말 아니었나?
사실 이 말은 처음부터 전기화학에서 쓰이던 개념은 아니었습니다.
전기가 흐르기 시작한 뒤, 전자는 눈에 보이지 않지만 분명히 오간다는 사실이 관찰되었고,
사람들은 그 흐름의 출발과 도착에 각각 이름을 붙일 필요를 느꼈습니다.
원래는 산소 이야기였다 – 산화의 어원
'산화(酸化, oxidation)'는 이름 그대로,
처음엔 산소(oxygen)와 결합하는 반응을 말했습니다.
- 예: 철이 녹슬다 → 철이 산소와 결합한다 → 산화되었다
이 단어는 18세기 라부아지에(Antoine Lavoisier)가 정립한 개념에서 유래하며,
‘산소를 잃는다’는 개념은 없었습니다. 오직 산소와 결합하는 것이었죠.
환원이라는 단어는 도대체 왜 ‘줄인다’는 뜻일까?
'환원(還元, reduction)'이란 단어는
금속 광석에서 금속을 ‘되찾는 과정’에서 유래한 말입니다.
고대 연금술이나 제련 기술에서는
녹슨 금속(산화된 상태)을 불로 가열하거나
다른 물질로 반응시켜 ‘원래의 금속 상태’로 되돌리는 과정이 있었습니다.
그걸 ‘환원(reduction)’, 즉 ‘되돌림’이라고 부른 거예요.
- 철광석(Fe₂O₃)을 가열하면 → 산소가 빠져나가고 → 금속 철(Fe)이 남는다
- 즉, 산소가 빠져나간다 → 환원되었다
그런데 전기화학이 오면서, 이 개념들이 완전히 바뀌었다
1800년대 들어 전기가 실험실에서 통제되기 시작하고,
볼타전지, 패러데이의 전기분해 같은 실험을 통해
사람들은 이런 사실을 알게 됩니다:
전기가 흐르면, 어떤 물질은 전자를 내어주고
또 어떤 물질은 그 전자를 받아간다
즉, 화학 반응은 전자의 교환으로 일어난다는 것이죠.
이제 더는 '산소'가 주인공이 아닙니다.
주인공은 '전자(e⁻)'입니다.

산화, 환원? 이름부터 헷갈린다!
처음 "산화"와 "환원"이라는 단어를 들으면 이런 반응이 많습니다:
“산소랑 관계 있는 거예요?”
“산화되면 나쁜 건가요?”
“환원은 회복되는 건가요?”
좋은 질문입니다.
사실 원래 화학에서 산화는 산소와 결합하는 것, 환원은 산소를 잃는 것을 의미했지만,
전기화학에서는 이렇게 정리합니다:
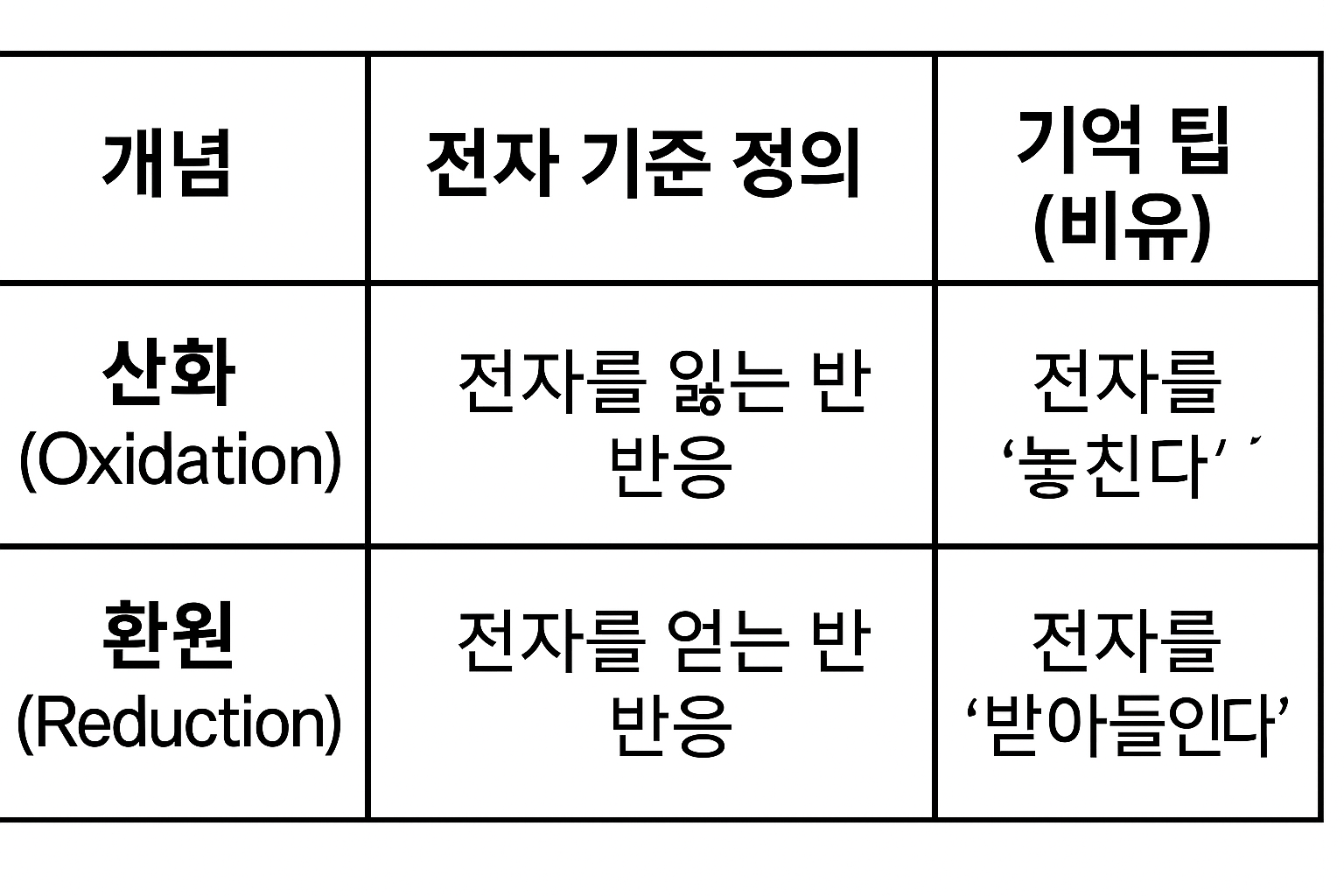
전기화학에서의 정의
❗ 전자(e⁻)가 핵심입니다.
누가 전자를 내어주고, 누가 받아가느냐가 산화-환원의 본질입니다.
볼타전지로 보는 산화/환원
이제 익숙한 '볼타전지(Zn–Cu)'를 떠올려볼게요.
- Zn (아연): 전자를 내놓습니다 → 산화
- Cu²⁺ (구리 이온): 전자를 받습니다 → 환원
즉, 전지 안에서 이런 일이 일어나는 거예요:
아연이 “전자 줄게” 하고 내놓고,
구리가 “고마워~” 하며 받아갑니다.
그 과정에서 전자가 흐르고, 전류가 만들어지는 것이죠.
전자가 오가는 무대: 전극
- 아연 전극(Zn): 산화가 일어나는 쪽 → 전자를 잃음 → 환원극(캐소드, cathode)
- 구리 전극(Cu): 환원이 일어나는 쪽 → 전자를 얻음 → 산화극(애노드, anode)
쉽게 생각하면,
산화는 전자를 방출하는 자리,
환원은 전자를 받아주는 자리입니다.
비유로 이해해보기
전자는 택배라고 생각해보세요.
- 아연은 택배를 ‘보내는 사람’ (산화)
- 구리 이온은 택배를 ‘받는 사람’ (환원)
- 전극은 택배가 오고가는 문 앞
택배(전자)가 왔다 갔다 하면서
그 과정에서 반응이 일어나고, 에너지가 발생합니다.
그게 바로 전기화학 반응이에요!
이 정의는 ‘산소’ 없이도 설명이 가능합니다.
그래서 수용액 속에서 금속이 녹거나,
전극에서 이온이 생성되거나 하는 모든 반응을
산화/환원이라는 말로 정리할 수 있게 되었죠.

이건 매우 중요한 포인트입니다:
그리고 사람들은 알게 됩니다:
산화와 환원은 항상 같이 일어난다
전자가 나가기만 하면 안 된다
반드시 받아주는 쪽도 있어야 한다
그래서 전기화학에서는 산화와 환원을 항상 “짝 반응”으로 다루게 됩니다.
이걸 영어로는 Redox reaction이라고 부르죠.
Reduction + Oxidation = Redox
산화만 일어날 수는 없습니다.
환원만 일어날 수도 없습니다.왜냐하면, 누군가 전자를 잃으면
반드시 누군가는 그 전자를 받아야 하기 때문입니다.
전기화학에서는 산화와 환원을 “짝 반응” 또는 '레독스 반응(REDOX, REDuction-OXidation)'이라고 부릅니다.
정리하면
- 산화: 전자를 잃는다 → 전자가 나간다 → 환원극(캐소드)에서 일어남
- 환원: 전자를 얻는다 → 전자가 들어온다 → 산화극(애노드)에서 일어남
- 둘은 동시에 일어나며 전류를 만든다
마무리하며
산화와 환원은
처음엔 산소와 관련된 이야기였고,
나중에는 금속을 되돌리는 제련의 용어였지만,
전자의 오고 감을 설명하는 가장 중요한 언어가 되었습니다.
전자가 오간다 = 반응이 일어난다
전자를 보내는 쪽 = 산화
전자를 받는 쪽 = 환원
이 개념은 지금도 모든 전기화학 반응의 중심에 있습니다.
그리고 이것이 바로 전기화학의 언어가 시작된 자리이기도 하죠.

'전기화학 개념 풀어쓰기' 카테고리의 다른 글
| 개념-8) 전위 랭킹쇼 — 누가 전자를 가장 갖고 싶어할까? (1) | 2025.06.16 |
|---|---|
| 개념-7) 산화와 환원의 방향, 전위로 읽기 (0) | 2025.06.15 |
| 개념-5) 전류 – 얼마나 많은 전자가 빨리 움직이는지를 말해주는 숫자 (0) | 2025.06.08 |
| 개념-4) 전위 – 전기가 ‘흐르기 시작하는 힘’에 대하여 (0) | 2025.06.08 |
| 개념-3) 혀 끝에서 시작된 전기: 볼타전지의 탄생과 직류 전기 시대 (1) | 2025.05.31 |